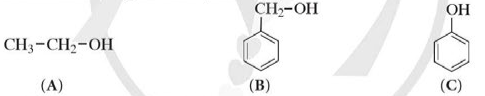
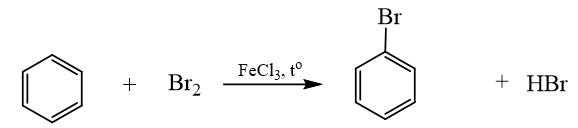
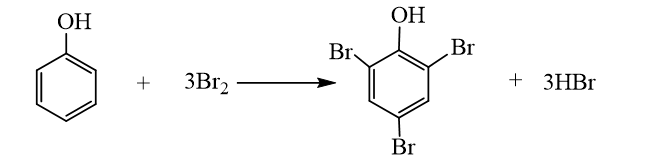
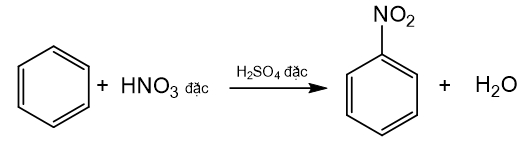
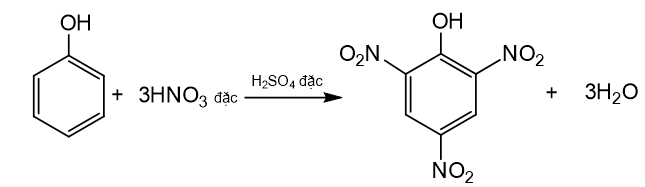
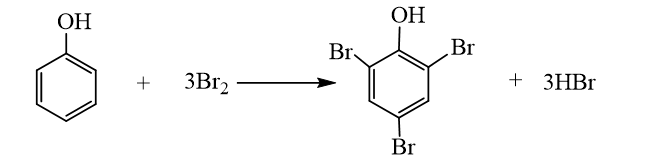
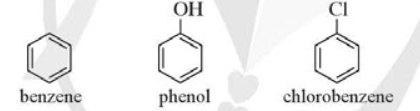
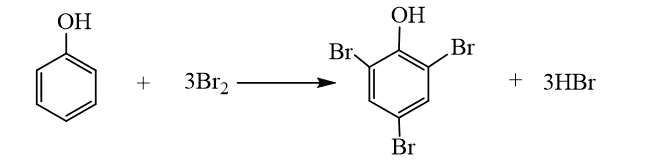
Bài 17: Phenol trang 116, 117, 118, 119, 120, 121 Hóa học 11 Cánh diềuCho ba chất có công thức cấu tạo dưới đây: a) Chất nào ở trên thuộc loại alcohol? b) Hợp chất (C) có những đặc điểm cấu tạo nào khác so với hai hợp chất (A) và (B)? c) Dự đoán tính chất hoá học của hợp chất (C) có khác (A) và (B) hay không. Tổng hợp đề thi giữa kì 2 lớp 11 tất cả các môn - Cánh diều Toán - Văn - Anh - Lí - Hóa - Sinh Lựa chọn câu để xem lời giải nhanh hơn CH tr 116 MĐ Cho ba chất có công thức cấu tạo dưới đây: a) Chất nào ở trên thuộc loại alcohol? b) Hợp chất (C) có những đặc điểm cấu tạo nào khác so với hai hợp chất (A) và (B)? c) Dự đoán tính chất hoá học của hợp chất (C) có khác (A) và (B) hay không. Phương pháp giải: a) Alcohol là những hợp chất hữu cơ trong phân tử có nhóm hydroxy (OH) liên kết trực tiếp với nguyên tử carbon no. b) Phenol là những hợp chất hữu cơ trong phân tử có một hay nhiều nhóm hydroxy liên kết trực tiếp với nguyên tử carbon của vòng benzene. c) Tính chất hóa học của alcohol: Phản ứng thế nguyên tử H trong nhóm –OH; Phản ứng thế nhóm –OH tạo ether; Phản ứng tách nước tạo alkene; Phản ứng oxi hóa không hoàn toàn và phản ứng cháy; Phản ứng của polyalcohol có nhiều nhóm –OH kề nhau. Tính chất hóa học của phenol: Tính acid yếu; Phản ứng thế nguyên tử H của nhân thơm. Lời giải chi tiết: a) (A) và (B) là alcohol. b) Hợp chất (C) có nhóm hydroxy (-OH) liên kết trực tiếp với vòng benzene. Hai hợp chất (A) và (B) có nhóm hydroxy (-OH) liên kết trực tiếp với carbon no. c) Hợp chất (C) có tính chất hóa học khác với tính chất hóa học của (A) và (B). CH tr 118 LT 1 Cho các chất có công thức sau: C6H5OH, C6H5CH3, C6H5Cl và các giá trị nhiệt độ sôi (không theo thứ tự là 110,6 °C, 131,7 °C, 181,8 °C. Hãy dự đoán nhiệt độ sôi tương ứng với mỗi chất trên. Giải thích. Phương pháp giải: Phân tử của dẫn xuất halogen phân cực nên chúng có nhiệt độ sôi cao hơn các hydrocarbon có phân tử khối tương đương. Do có nhóm –OH trong phân tử nên phenol tạo ra liên kết hydrogen giữa các phân tử. Do vậy, phenol có nhiệt độ sôi cao hơn các aryl halide có phân tử khối tương dương. Lời giải chi tiết: Giải thích: + Liên kết C – Cl trong phân tử C6H5Cl phân cực nên C6H5Cl có nhiệt độ sôi cao hơn phân tử C6H5CH3. + Nhóm –OH trong phân tử C6H5OH tạo ra liên kết hydrogen. Do vậy, C6H5OH có nhiệt độ sôi cao hơn C6H5Cl. Vậy nhiệt độ sôi của các chất theo thứ tự giảm dần là: C6H5OH, C6H5Cl, C6H5CH3. CH tr 118 CH 1 Nhận xét đặc điểm cấu tạo của phân tử phenol về nhóm chức và gốc hydrocarbon. Từ đó dự đoán về tính chất hoá học ở nhóm chức (so sánh với alcohol) và ở gốc hydrocarbon (so sánh với benzene). Phương pháp giải: Tính chất hóa học của phenol: Tính acid yếu; Phản ứng thế nguyên tử H của nhân thơm. Lời giải chi tiết: Trong phân tử phenol, nhóm –OH liên kết trực tiếp với vòng benzene. Chính nhờ có sự liên kết này, vòng benzene trở thành nhóm hút electron, làm giảm mật độ electron ở nguyên tử oxygen và tăng sự phân cực của liên kết O−H (so với trong phân tử alcohol); đồng thời làm tăng mật độ electron trong vòng benzene, nhất là ở các vị trí ortho và para. Phenol có tính acid mạnh hơn alcohol và phản ứng thế nguyên tử H của vòng benzene ở phenol xảy ra dễ hơn benzene. CH tr 118 LT 2 Hãy dẫn ra các phương trình hoá học để chứng minh rằng tính acid của phenol mạnh hơn của alcohol. Phương pháp giải: Phenol thể hiện tính acid yếu. Dung dịch phenol không làm đổi màu quỳ tím. + Phản ứng với dung dịch NaOH: Phenol ít tan trong nước nhưng tan tốt trong dung dịch sodium hydroxide. + Phản ứng với dung dịch sodium carbonate: Phenol tan được trong dung dịch muối sodium carbonate. Lời giải chi tiết: Tính acid của phenol mạnh hơn của alcohol vì: Phenol có thể phản ứng được với kim loại kiềm, dung dịch base, muối sodium carbonate trong khi alcohol chỉ phản ứng được với kim loại kiềm, không phản ứng được với dung dịch base, muối sodium carbonate. C6H5OH + NaOH → C6H5ONa + H2O C6H5OH +Na2CO3 C6H5ONa +NaHCO3 CH tr 119 TN 1 Thí nghiệm 1. Phản ứng của phenol và dung dịch NaOH Chuẩn bị: Phenol ở dạng huyền phù, dung dịch NaOH 1M; ống nghiệm. Tiến hành: Chuẩn bị một ống nghiệm chứa khoảng 1 mL phenol dạng huyền phù. Nhỏ từ từ khoảng 2 mL dung dịch sodium hydroxide 1 M vào ống nghiệm. Lắc đều ống nghiệm. Yêu cầu: Quan sát, mô tả hiện tượng xảy ra và giải thích. Phương pháp giải: Phenol ít tan trong nước nhưng tan tốt trong dung dịch sodium hydroxide. Lời giải chi tiết: - Hiện tượng: Dung dịch ở dạng huyền phù, màu trắng đục tan thành dung dịch trong suốt. - Giải thích: Phenol phản ứng với dung dịch sodium hydroxide tạo thành dung dịch muối tan trong suốt sodium phenolate (C6H5ONa). - Phương trình: C6H5OH + NaOH → C6H5ONa + H2O CH tr 119 TN 2 Thí nghiệm 2. Phản ứng của phenol với dung dịch Na2CO3 Chuẩn bị: Phenol ở dạng huyền phù, dung dịch Na2CO3 1 M; ống nghiệm. Tiến hành: Cho vào ống nghiệm khoảng 1 mL phenol dạng huyền phù. Nhỏ từ từ khoảng 2 mL dung dịch sodium carbonate 1 M vào ống nghiệm. Lắc đều ống nghiệm. Yêu cầu: Quan sát, mô tả hiện tượng xảy ra và giải thích. Phương pháp giải: Phenol tan được trong dung dịch muối sodium carbonate. Lời giải chi tiết: - Hiện tượng: Dung dịch ở dạng huyền phù, màu trắng đục tan thành dung dịch trong suốt. - Giải thích: Phenol phản ứng với dung dịch sodium carbonate tạo thành dung dịch muối tan trong suốt gồm sodium phenolate (C6H5ONa) và sodium hydrocarbonate (NaHCO3). - Phương trình: C6H5OH +Na2CO3 C6H5ONa + NaHCO3 CH tr 119 LT 3 Hãy dẫn ra các phương trình hoá học để chứng minh phản ứng thế nguyên tử H ở vòng benzene trong phenol dễ hơn benzene. Phương pháp giải: - Phenol phản ứng bromine: Nhỏ nước bromine vào dung dịch phenol, thấy xuất hiện kết tủa trắng, do có phản ứng sinh ra 2,4,6-tribromophenol. - Phản ứng với dung dịch HNO3 đặc: phenol phản ứng với dung dịch nitric acid đặc (xúc tác sulfuric acid đặc) thu được kết tủa vàng là picric acid (hay 2,4,6-trinitrophenol). Lời giải chi tiết: - Phản ứng thế bromine vào vòng thơm của benzene và phenol: + Benzene phản ứng thế với bromine cần xúc tác FeCl3, đun nóng. 1 nguyên tử Br thế 1 nguyên tử H ở vòng thơm. + Phenol phản ứng thế với bromine ở điều kiện thường. 3 nguyên tử Br thế được 3 nguyên tử H ở vòng thơm. - Phản ứng thế nhóm nitro vào vòng thơm của benzene và phenol: + Benzene phản ứng với nitric acid đặc (xúc tác sulfuric acid đặc), 1 nhóm NO2 thế 1 nguyên tử H trên vòng thơm. + Phenol phản ứng với nitric acid đặc (xúc tác sulfuric acid đặc), 3 nhóm NO2 thế 3 nguyên tử H trên vòng thơm. => Phản ứng thế H vào vòng thơm của phenol xảy ra dễ hơn benzene. CH tr 119 TN 3 Thí nghiệm 3. Phản ứng của phenol với nước bromine Chuẩn bị: Dung dịch phenol 5%, nước bromine bão hoà, ống nghiệm. Tiến hành: Cho 0,5 mL dung dịch phenol 5% vào ống nghiệm và thêm vài giọt nước bromine bão hòa. Lắc đều ống nghiệm. Yêu cầu: Quan sát, mô tả hiện tượng xảy ra và giải thích. Phương pháp giải: Phenol phản ứng bromine: Nhỏ nước bromine vào dung dịch phenol, thấy xuất hiện kết tủa trắng, do có phản ứng sinh ra 2,4,6-tribromophenol. Lời giải chi tiết: - Hiện tượng: Nước bromine mất màu và xuất hiện kết tủa trắng. - Giải thích: Phenol phản ứng bromine, làm nước bromine mất màu, tạo kết tủa trắng 2,4,6-tribromophenol.
CH tr 119 LT 4 Có ba ống nghiệm chứa các chất lỏng sau: dung dịch propanol, dung dịch phenol và benzene. Hãy đề xuất một thuốc thử để nhận biết ống nghiệm chứa dung dịch phenol. Phương pháp giải: Sử dụng benzene để nhận biết dung dịch propanol, dung dịch phenol và benzene. Lời giải chi tiết: - Đánh số thứ tự cho từng ống nghiệm. Trích dung dịch làm mẫu thử đánh số thứ tự tương ứng. - Nhỏ vào ba mẫu thử chứa các chất lỏng cần nhận biết, mỗi ống vài giọt bromine: + Ống nghiệm chứa phenol làm nước bromine mất màu và xuất hiện kết tủa trắng. + Phương trình hóa học:
CH tr 120 TN 4 Thí nghiệm 4. Phản ứng của phenol với nitric acid dặc Cho khoảng 0,5 g phenol và 1,5 mL dung dịch H2SO4 đặc vào ống nghiệm, sau đó đun nóng hỗn hợp để thu được chất lỏng đồng nhất. Làm lạnh ống nghiệm rồi nhỏ từ từ khoảng 1 mL dung dịch HNO3 đặc vào hỗn hợp, lắc đều. Hỗn hợp trong ống nghiệm nhuốm màu đỏ tối. Đun cách thuỷ hỗn hợp trong 15 phút. Sau đó để nguội rồi rót hỗn hợp vào cốc đựng 20 mL nước lạnh sẽ thấy picric acid tách ra ở dạng kết tủa màu vàng. Yêu cầu: Viết phương trình hóa học và giải thích hiện tượng xảy ra. Phương pháp giải: Phản ứng với dung dịch HNO3 đặc: phenol phản ứng với dung dịch nitric acid đặc (xúc tác sulfuric acid đặc) thu được kết tủa vàng là picric acid (hay 2,4,6-trinitrophenol). Lời giải chi tiết: - Giải thích: Hỗn hợp trong ống nghiệm nhuốm màu đỏ tối vì quá trình phản ứng giữa phenol và nitric acid tạo khói và dung dịch có màu đỏ tối. Sản phẩm thu được ở dạng kết tủa vàng là picric acid (hay 2,4,6-trinitrophenol). - Phương trình hóa học:
CH tr 120 CH 4 Hãy trình bày một số ứng dụng của phenol trong thực tiễn. Phương pháp giải: Trong thực tiễn, phenol được dùng để sản xuất nhựa, sản xuất phẩm nhuộm, thuốc nổ; tẩy uế, sát trùng,… Lời giải chi tiết: Phenol được sử dụng nhiều trong công nghiệp hoá chất và y học. Phenol là nguyên liệu chính để sản xuất bisphenol A, nhựa phenol-formaldehyde hay poly(phenol-formaldehyde). Phenol được dùng để sản xuất phẩm nhuộm, sản xuất thuốc nổ (2,4,6-trinitrophenol), chất diệt có 2,4-D (2,4-dichlorophenoxyacetic acid), chất diệt nấm mốc (các đồng phân của nitrophenol),... Thuốc xịt chloraseptic chứa 1,4% phenol được dùng làm thuốc chữa đau họng. Bài tập Bài 1 Trong các chất có công thức sau, chất nào có nhiệt độ sôi cao nhất?
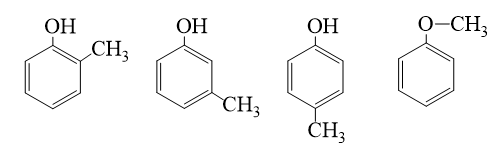
Phương pháp giải: Phân tử của dẫn xuất halogen phân cực nên chúng có nhiệt độ sôi cao hơn các hydrocarbon có phân tử khối tương đương. Do có nhóm –OH trong phân tử nên phenol tạo ra liên kết hydrogen giữa các phân tử. Do vậy, phenol có nhiệt độ sôi và nhiệt độ nóng chảy cao hơn các aryl halide có phân tử khối tương đương Lời giải chi tiết: Vì chlorobenzene phân cực nên chlorobenzene có nhiệt độ sôi cao hơn benzene. Phân tử phenol có nhóm hydroxy trong phân tử nên giữa các phân tử phenol có liên kết hydrogen, do đó phenol có nhiệt độ sôi cao hơn chlorobenzene. Vậy chất có nhiệt độ sôi cao nhất là phenol. Bài tập Bài 2 Hãy viết công thức cấu tạo các chất chứa vòng benzene có cùng công thức phân tử C7H8O Phương pháp giải: Viết các đồng phân của cresol và đồng phân ether. Lời giải chi tiết: Công thức cấu tạo các chất chứa vòng benzene có cùng công thức phân tử C7H8O:
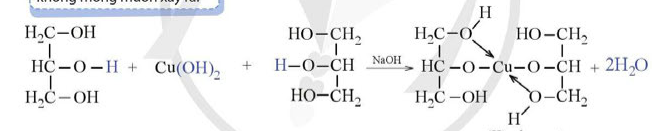
Bài tập Bài 3 Trình bày cách phân biệt các dung dịch sau: dung dịch phenol, dung dịch ethanol, dung dịch glycerol. Phương pháp giải: - Phenol phản ứng với nước bromine tạo kết tủa trắng. - Glycerol hòa tan Cu(OH)2 tạo phức màu xanh lam. Lời giải chi tiết: - Đánh số thứ tự cho từng dung dịch. Trích dung dịch làm mẫu thử đánh số thứ tự tương ứng. - Nhỏ vài giọt nước bromine vào từng mẫu thử: + Mẫu thử chứa phenol có hiện tượng làm mất màu nước bromine và tạo thành kết tủa trắng. + Mẫu thử chứa ethanol và glycerol không có hiện tượng. - Tiếp tục trích dung dịch (của nhóm mẫu thử không hiện tượng) làm mẫu thử và đánh số thứ tự tương ứng. - Nhỏ vài giọt dung dịch sodium hydroxide và copper(II) sulfate vào hai mẫu thử, lắc đều ống nghiệm. Mẫu thử chứa glycerol sẽ xuất hiện kết tủa xanh lam rồi kết tủa tan dần tạo thành dung dịch xanh lam. Mẫu thử chứa ethanol sẽ xuất hiện kết tủa xanh lam nhưng kết tủa không bị tan. * Phương trình hóa học: CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4 Bài tập Bài 4 Rutin có nhiều trong hoa hoè. Rutin có tác dụng làm bền vững thành mạch, chống co thắt, chống phóng xạ tia X, chống viêm cầu thận cấp. Rutin có công thức phân tử C27H30O16 và công thức cấu tạo như bên: a) Phân tử rutin có bao nhiêu nhóm OH alcohol và bao nhiêu nhóm –OH phenol? b) Có hai phương pháp tách rutin từ hoa hoè như sau: Phương pháp 1: Hoa hoè xử lí bằng dung dịch sodium hydroxyde. Lọc, acid hoá phần nước lọc, thu được rutin. Phương pháp 2: Chiết rutin từ hoa hoè bằng nước nóng sau đó để nguội, rutin sẽ tách ra. Em hãy cho biết mỗi phương pháp trên đã dựa vào tính chất nào của rutin. Phương pháp giải: a) Alcohol là những hợp chất hữu cơ trong phân tử có nhóm hydroxy (OH) liên kết trực tiếp với nguyên tử carbon no. Phenol là những hợp chất hữu cơ trong phân tử có một hay nhiều nhóm hydroxy liên kết trực tiếp với nguyên tử carbon của vòng benzene. b) Phenol tan vô hạn trong nước ở 66 oC. Tính chất hóa học của phenol: Tính acid yếu; Phản ứng thế nguyên tử H của nhân thơm. Lời giải chi tiết: a) Rutin có 6 nhóm OH alcohol và 4 nhóm –OH phenol. b) Phương pháp 1 dựa vào tính acid của nhóm chức phenol trong phân tử rutin, phản ứng với dung dịch base (sodium hydroxyde). Phương pháp 2 dựa vào tính tan nhiều trong nước nóng, ít tan trong nước lạnh của nhóm chức phenol trong phân tử rutin.
|