Bài 17. Nguyên tố và đơn chất halogen trang 99, 100, 101, 102, 103, 104, 105, 106, 107, 108 Hóa 10 Cánh diềuTải vềVì sao nước chlorine được sử dụng phổ biến để khử trùng, sát khuẩn? Dựa vào xu hướng biến đổi tính chất của các đơn chất halogen trong bảng 17.3, hãy dự đoán về thể (trạng thái) của đơn chất astatine ở điều kiện thường. Giải thích Trong điều kiện thường, halogen nào ở thể rắn? Vì sao Tổng hợp đề thi giữa kì 2 lớp 10 tất cả các môn - Cánh diều Toán - Văn - Anh - Lí - Hóa - Sinh Lựa chọn câu để xem lời giải nhanh hơn Tải về CH tr 99 MĐ
Lời giải chi tiết: - Nước chlorine có thành phần là HCl và HClO có tính oxi hóa mạnh => Nước chlorine có tính tẩy màu được dùng để khử trùng và sát khuẩn, tẩy trắng sợi, vải, giấy CH tr 101 LT
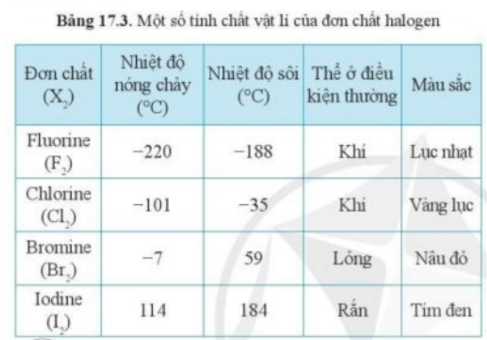
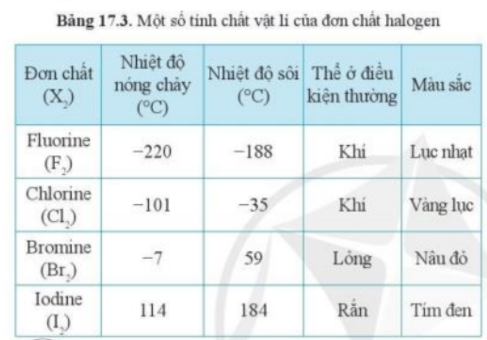
Phương pháp giải: Trong bảng 17.3, thể của các halogen ở điều kiện thường biến đổi từ khí → lỏng → rắn Lời giải chi tiết: - Theo bảng 17.3, xu hướng biến đổi trạng thái của các halogen ở điều kiện thường từ: khí → lỏng → rắn - Mà astatine đứng dưới cùng trong nhóm halogen => Astatine tồn tại ở thể rắn trong điều kiện thường - Giải thích: Do sự tăng khối lượng phân tử và sự tăng tương tác van dể Waals CH tr 101 LT
Phương pháp giải: - Dựa vào thông tin bảng 17.3 - Giải thích: Khối lượng phân tử, sự tăng tương tác van der Waals Lời giải chi tiết: - Quan sát Bảng 17.3, nhận thấy trong điều kiện thường có Iodine (I2) là ở thể rắn - Giải thích: + Khối lượng phân tử cao + Lực tương tác van der Waals giữa phân tử iodine mạnh CH tr 102 LT
Phương pháp giải: - Các nguyên tố halogen có 7 electron ở lớp ngoài cùng - Nguyên tố calcium có 2 electron ở lớp ngoài cùng Lời giải chi tiết: - Nguyên tử Fluorine có 7 electron ở lớp ngoài cùng => Nhận 1 electron từ nguyên tử Calcium để đạt cấu hình electron của khí hiếm - Nguyên tử Calcium có 2 electron ở lớp ngoài cùng => Nhường 2 electron cho 2 nguyên tử Fluorine để đạt cấu hình electron của khí hiếm CH tr 102 LT
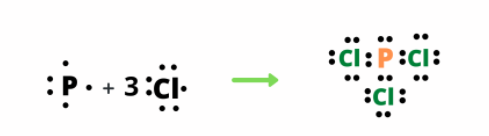
Phương pháp giải: - Nguyên tử Phosphorus có 5 electron ở lớp ngoài cùng => Có xu hướng nhận thêm 3 electron - Nguyên tử Chlorine có 7 electron ở lớp ngoài cùng => Có xu hướng nhận thêm 1 electron Lời giải chi tiết: - Trong phân tử phosphorus trichloride gồm 2 nguyên tố: P và Cl + Nguyên tử P có 5 electron ở lớp ngoài cùng => Góp chung 3 electron độc thân để hình thành 3 liên kết cộng hóa trị + Nguyên tử Cl có 7 electron ở lớp ngoài cùng => 3 nguyên tử Cl, mỗi nguyên tử góp chung 1 electron độc thân để hình thành 3 liên kết cộng hóa trị với P. => Khi đó, quanh P và Cl đều có 8 electron như khí hiếm Argon. - Công thức Lewis của phân tử: CH tr 103 LT
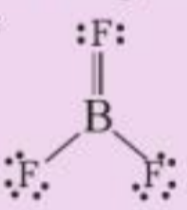
Phương pháp giải: a) Phương trình hóa học: B + F2 → ? b) Liên kết đơn còn gọi là liên kết σ, liên kết đôi gồm 1 liên kết σ và 1 liên kết п Lời giải chi tiết: a) Phương trình hóa học: 2B + 3F2 → 2BF3 b) Trong phân tử BF3 có 2 liên kết đơn, 1 liên kết đôi (gồm 1 liên kết σ và 1 liên kết п) => Trong phân tử BF3 có 3 liên kết σ và 1 liên kết п CH tr 104 TH
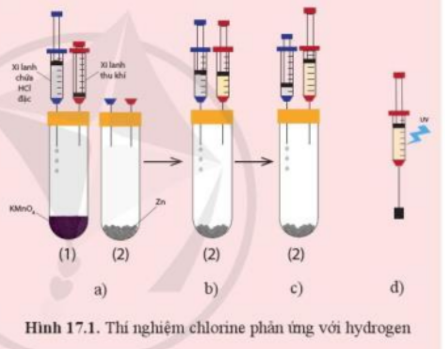
Phương pháp giải: - H2 tác dụng với Cl2 gây hiện tượng nổ khi đun nóng hoặc nổ ngay ở nhiệt độ thường khi được chiếu tia tử ngoại - Không có hiện tượng như thí nghiệm trên Lời giải chi tiết: a) - Ở Bước 2: Ta thu được khí chlorine - Ở Bước 4: Ta thu được khí hydrogen => Trong xi – lanh là hỗn hợp kí chlorine và hydrogen - Khi chiếu đèn tử ngoại vào xi – lanh hoặc dùng ngọn lửa hơ nhẹ bên ngoài xi - lanh chứa hỗn hợp khí chlorine và hydrogen sẽ gây ra hiện tượng nổ - Phương trình hóa học: H2 + Cl2 → 2HCl b) Nếu thay khí chlorine bằng hơi iodine thì phản ứng giữa hơi iodine và hydrogen không xảy ra hiện tượng như trên. - Giải thích: Phản ứng giữa H2 và I2 cần đun nóng để phản ứng diễn ra, là phản ứng thuận nghịch, tạo hỗn hợp gồm HI sinh ra và lượng H2, I2 còn lại. Khả năng phản ứng kém nên không có hiện tượng nổ H2 + I2 \( \rightleftharpoons \) 2HI CH tr 105 TH
Phương pháp giải: Trong dung dịch, các halogen có tính oxi hóa mạnh hơn sẽ phản ứng với muối halide của halogen có tính oxi hóa yếu hơn để tạo ra các halogen có tính oxi hóa yếu hơn Lời giải chi tiết: - Thí nghiệm 1: + Khi cho nước chlorine màu vàng rất nhạt vào dung dịch sodium bromide không màu thì tạo ra dung dịch màu vàng nâu của bromine: Cl2(aq) + 2NaBr(aq) → 2NaCl(aq) + Br2(aq) + Khi nhỏ 2 mL cyclohexane vào ống nghiệm, quan sát thấy màu vàng nâu của bromine nhạt dần do bromine tham gia phản ứng với cyclohexane: Br2 + C6H12 → HBr + C6H11Br - Thí nghiệm 2: + Khi cho nước bromine màu vàng vào dung dịch sodium iodine không màu thì tạo ra dung dịch màu vàng: Br2(aq) + 2NaI(aq) → 2NaBr(aq) + I2(aq) + Khi cho thêm 2 mL cyclohexane thấy màu dung dịch nhạt dần do bromine tham gia phản ứng với cyclohexane: Br2 + C6H12 → HBr + C6H11Br + Khi thêm tiếp vài giọt hồ tinh bột thì thấy dung dịch từ màu vàng chuyển sang màu xanh tím do iodine tác dụng với hồ tinh bột CH tr 105 CH
Phương pháp giải: Phản ứng hóa học: Br2(aq) + H2O(l) \( \rightleftharpoons \) HBr(aq) + HBrO(aq) Lời giải chi tiết: Sau khi nhỏ nhanh vài giọt bromine vào ống nghiệm chứa nước, dung dịch bromine có những chất: Br2, H2O, HBr, HBrO. Br2(aq) + H2O(l) \( \rightleftharpoons \) HBr(aq) + HBrO(aq) - Vì phản ứng xảy ra thuận nghịch nên trong dung dịch có cả chất tham gia và chất sản phẩm CH tr 106 TH
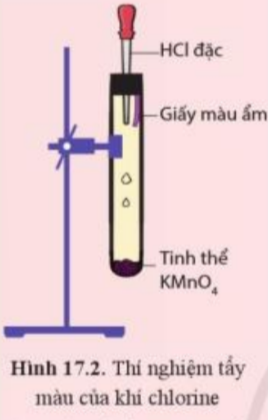
Phương pháp giải: - Phản ứng tạo ra khí chlorine, khí chlorine kết hợp với nước tạo ra dung dịch có tính tẩy màu Lời giải chi tiết: - Hiện tượng: Xuất hiện khí màu vàng và giấy màu ẩm bị nhạt màu dần rồi mất màu - Giải thích: + Khi nhỏ HCl đặc vào tinh thể KMnO4, sản phẩm tạo thành có khí chlorine: 2KMnO4 + 16HCl → 2MnCl2 + 2KCl + 5Cl2 + 8H2O + Khí chlorine tác dụng với nước ở giấy màu ẩm tạo thành hỗn hợp có tính tẩy màu: HCl và HClO Cl2(aq) + H2O(l) \( \rightleftharpoons \) HCl(aq) + HClO(aq) => Dung dịch này còn được gọi là dung dịch nước chlorine, có tính tẩy màu, sát khuẩn CH tr 106 VD
Phương pháp giải: Halogen là những chất oxi hóa mạnh Lời giải chi tiết: - Halogen là những chất oxi hóa mạnh, dễ dàng tác dụng với các chất khác trong tự nhiên: tác dụng với nước, hydrogen,… => Trong tự nhiên, các halogen không tồn tại ở dạng đơn chất mà tồn tại ở dạng hợp chất Bài tập 1
Phương pháp giải: Các halogen có tính oxi hóa mạnh hơn sẽ phản ứng với muối halide của halogen có tính oxi hóa yếu hơn để tạo ra các halogen có tính oxi hóa yếu hơn Lời giải chi tiết: Cl2 + 2NaBr → 2NaCl + Br2 => Cl2 có tính oxi hóa mạnh hơn sẽ phản ứng với NaBr tạo thành halogen có tính oxi hóa yếu hơn là Br2 => Chlorine có tính oxi hóa mạnh hơn bromine Bài tập 2
Phương pháp giải: - Chất tẩy rửa phổ biến là nước Javel: NaCl và NaClO - Để sản xuất được hydrogen chloride cần: Cl2 và H2 Lời giải chi tiết: - Chất tẩy rửa phổ biến là nước Javel gồm có NaCl và NaClO => Hai chất tác dụng với nhau để tạo thành nước Javel là: NaOH và Cl2 - Vì A ở dạng dung dịch, Y ở dạng khí => A là dung dịch NaOH, Y là khí Cl2 - Để sản xuất được hydrogen chloride cần: Cl2 và H2 - Mà Y là khí Cl2 => X là khí H2 a) Công thức hóa học của A, X, Y lần lượt là: NaOH, H2, Cl2 b) Phương trình hóa học 2NaCl (aq) + 2H2O (l) → 2NaOH (aq) + H2 (g) + Cl2 (g) (*) Bài tập 3
Phương pháp giải: - Trong nhóm halogen, đi từ F đến I, tính oxi hóa giảm dần - Trong nhóm halogen, đi từ F đến I, màu sắc đậm dần Lời giải chi tiết: a) Trong nhóm halogen, đi từ F đến I có độ âm điện giảm dần => Tính oxi hóa giảm dần => Tính oxi hóa của nguyên tử astatine yếu hơn so với nguyên tử iodine b) Trong nhóm halogen, đi từ F đến I có màu sắc của các đơn chất đậm dần => Đơn chất astatine có màu đậm hơn so với đơn chất iodine Bài tập 4
Phương pháp giải:
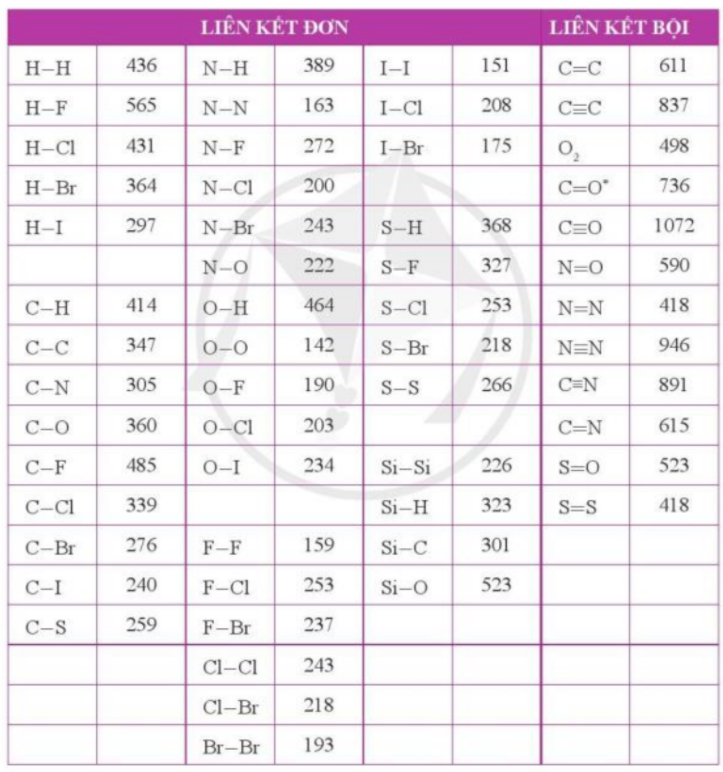
a) ∆rH0298 = Eb(F2) + Eb(H2) – 2xEb(HF) ∆rH0298 = Eb(O2) + 2xEb(H2) – 2x2xEb(OH) b) Giá trị biến thiên enthalpy nào âm hơn thì phản ứng đó diễn ra thuận lợi hơn Lời giải chi tiết: a) - Xét phản ứng: F2(g) + H2(g) → 2HF (g) + Ta có: ∆rH0298 = Eb(F2) + Eb(H2) – 2xEb(HF) = 159 + 436 – 2x565 = -535 (kJ/mol) - Xét phản ứng: O2(g) + 2H2(g) → 2H2O(g) + Ta có: ∆rH0298 = Eb(O2) + 2xEb(H2) – 2x2xEb(OH) = 142 + 2x436 – 2x2x464 = -842 (kJ/mol) b) Giá trị biến thiên enthalpy của phản ứng (2) âm hơn giá trị biến thiên enthalpy của phản ứng (1) => Phản ứng oxi hóa – khử (2) diễn ra thuận lợi hơn Bài tập 5
Phương pháp giải: a) Chlorine có mùi xốc b) Ngăn ngừa sự tái nhiễm của vi khuẩn c) Tham khảo phần cuối của đoạn văn trên Lời giải chi tiết: a) Chlorine có mùi xốc, nên khi sử dụng nước sinh có chlorine, chúng ta sẽ ngửi thấy mùi của nước chlorine b) Trong quá trình khử trùng, người ta phải cho một lượng chlorine dư vào nước sinh hoạt. Lượng chlorine dư trong nước sinh hoạt còn có tác dụng ngăn ngừa sự tái nhiễm của vi khuẩn trong quá trình phân phối trong đường ống dẫn nước và trữ nước tại nhà c) Một số phương pháp để loại bỏ khí chlorine dư trong nước sinh hoạt: - Sử dụng máy lọc nước than hoạt tính - Phơi chậu nước ra ngoài ánh nắng mặt trời => Tia cực tím với cường độ cao vào nước cùng làm giảm lượng chlorine - Sử dụng máy lọc nước RO (thẩm thấu ngược) cũng có thể giúp loại bỏ lượng chlorine trong nước
|