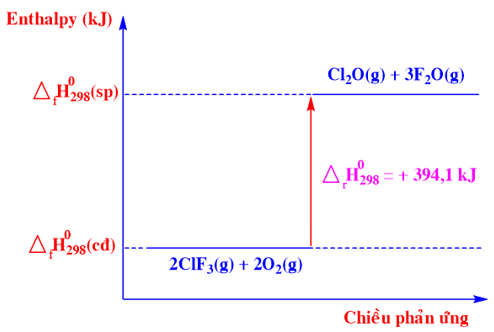
Phương trình nhiệt hoá học nào sau đây ứng với sơ đồ biểu diễn biến thiên enthalpy của phản ứng sau:
- A.
Cl2O (g) + 3F2O (g) → 2ClF3 (g) + 2O2 (g) \({\Delta _r}H_{298}^0\) = -394,10 kJ
- B.
Cl2O (g) + 3F2O(g) → 2ClF3 (g) + 2O2 (g) \({\Delta _r}H_{298}^0\) = +394,10 kJ
- C.
2ClF3 (g) + 2O2 (g) → Cl2O (g) + 3F2O (g) \({\Delta _r}H_{298}^0\) = +394,10 kJ
- D.
2ClF3 (g) + 2O2 (g) → Cl2O (g) + 3F2O (g) \({\Delta _r}H_{298}^0\) = -394,10 kJ
Đáp án : C
Dựa vào sơ đồ biểu diễn biến thiên enthalpy
Chất tham gia: ClF3(g) và O2(g)
Chất sản phẩm: Cl2O(g) và F2O(g)
Biến thiên enthalpy của phản ứng là: \({\Delta _r}H_{298}^0\) = +394,10 kJ
=>2ClF3 (g) + 2O2 (g) → Cl2O (g) + 3F2O (g) \({\Delta _r}H_{298}^0\) = +394,10 kJ
Các bài tập cùng chuyên đề
Cho phản ứng: 2SO2(g) + O2(g) 2SO3(g). Nồng độ của sulfur dioxide tăng 2 lần và oxygen tăng 3 lần thì tốc độ phản ứng tăng lên bao nhiêu lần?
Hệ số nhiệt độ của tốc độ phản ứng bằng 3,5. Ở 150C tốc độ phản ứng này bằng 0,2 s-1. Tính tốc độ phản ứng ở 400C.
Từ MnO2, HClđặc, Fe hãy viết các phương trình phản ứng điều chế Cl2, FeCl2 và FeCl3.
Cho 5 gam kẽm viên vào cốc đựng 50 ml dung dịch H2SO4 4M ở nhiệt độ thường (25oC).
Trường hợp nào tốc độ phản ứng không đổi ?
Phản ứng chuyển hoá giữa hai dạng đơn chất của phosphorus (P):
P(s, đỏ) \( \to \)P (s, trắng) \({\Delta _{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\) = 17,6 kJ
Điều này chứng tỏ phản ứng:
Cho 5,6 gam kim loại sắt vào dung dịch hydrochloric acid, sau phản ứng thu được V lít khí ở đkc. Giá trị của V là:
Từ HF đến HI, tính acid của các dung dịch hydrogen halide biến đổi như thế nào?
Cho biến thiên enthalpy của phản ứng sau ở điều kiện chuẩn:
CO(g) + 1/2O2(g) → CO2(g) \({\Delta _r}H_{298}^0 = - 283,0kJ\)
Biết nhiệt tạo thành chuẩn của CO2 là -393,5 kJ/mol. Nhiệt tạo thành chuẩn của CO là












