Đề bài
Khi đốt cháy hoàn toàn 0,35 mol hỗn hợp khí gồm CH4, C2H6, C3H8 thu được 0,75 mol khí CO2 và x gam H2O. Giá trị của x là:
- A.
6,3
- B.
13,5
- C.
18,0
- D.
19,8
Đáp án : D
Phương pháp giải :
Dựa vào phản ứng đốt cháy alkane: n H2O – n CO2 = n alkane
Lời giải chi tiết :
n H2O – n CO2 = n alkane => n H2O = 0,75 + 0,35 = 1,1 mol => m H2O = 19,8g
Đáp án D
Các bài tập cùng chuyên đề
Bài 4 :
Phân tích nguyên tố của hợp chất X cho kết quả: 84%C; 16%H về khối lượng. Phân tử khối của hợp chất X được xác định thông qua kết quả phổ khối lượng với peak ion phân tử có giá trị m/z lớn nhất là 100. Công thức của X là
Bài 5 :
Cho isopentane tác dụng với Cl2 theo tỉ lệ số mol 1: 1, số sản phẩm monochloro tối đa thu được là
Bài 8 :
Alkane Y phản ứng với chlorine tạo ra 2 dẫn xuất monochloro có tỉ khối hơi so với H2 bằng 39,25. Tên của Y là:













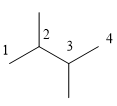 có tên gọi là:
có tên gọi là: